時論廣場》總統的疫苗 不是所有人的天菜(邱淑媞)
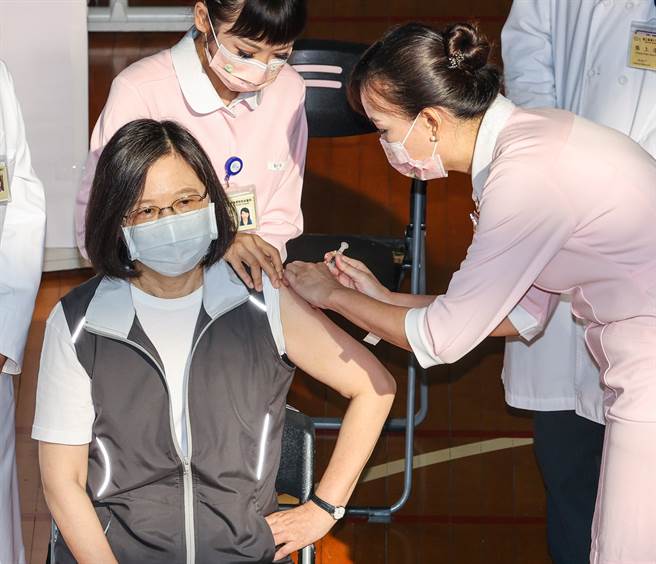
高端疫苗開打,總統蔡英文(左)23日一早前往臺大醫學院體育館,捲起衣袖,率先完成接種高端疫苗。(圖/中央社)
攸關疫戰成敗的疫苗發展,823這天於太平洋兩端都掀開新頁: 一方是美國食藥署(FDA)批准美德混血的輝瑞/BNT疫苗成爲全球第一支拿到完整藥證的新冠疫苗,16歲以上的民衆得逕由醫療機構接種;另一方的臺灣則是由蔡總統開打尚未做第三期臨牀試驗即獲EUA的本土疫苗,展開獨打高端的第六輪接種,並讓30歲以下年輕族羣開始預約接種。一進化、一退化的生技落差,形成強烈對照。
在美國有逾2億劑接種數據的輝瑞/BNT復必泰疫苗,經3個多月嚴格審查,確認「安全性、有效性和品管」三者皆有信心後通過完整藥證,供醫療機構、學校、職場爲16歲以上的民衆接種,不須再經政府提供。
這是一個分水嶺。此後,全球新冠疫苗之科學實證與覈准等級可分爲四級,一是擁有完整數據、完整藥證者(目前爲BNT);二是獲世界衛生組織(WHO)審查列表者(俗稱國際認證──BNT、莫德納、嬌生、AZ五廠、科興、國藥);三是其他有三期試驗且獲至少一國EUA者(例如俄羅斯衛星五號等,共15款);四是全球唯一的、沒有三期試驗就獲EUA開打者──臺灣覈准的高端。而與高端同屬重組蛋白疫苗的Novavax,雖其三期試驗對變種病毒亦有高度保護力,卻因顧慮自身量產品管未臻成熟,寧可股價下跌,也堅持延後對美國提出EUA申請。
臺灣以特製的免疫橋接標準,跳過第三期試驗,超前核準本土疫苗,猶如未做過實彈測試的頭盔,未確知保護力就要全民配佩戴上戰場。橋接所採用的免疫指標也只看半套──美國、歐盟、世界衛生組織都要求免疫反應必須同時看B細胞抗體效價與T細胞免疫反應,後者關乎重症保護力,也涉及抗體依賴性免疫傷害之風險。高端未提出人體T細胞免疫反應數據,對Delta變種病毒的有效性、最適劑量、有無罕見重大副作用等亦遭質疑,而品管上量產能力不足、難保確效,更被列入審查決議。與Novavax迥然不同的是,政府仍予強行通過、開打,導致無法掌握供貨數量的窘境。
這些都是在審查高端時已列入公文紀錄的,何須等到其他廠商提出質疑?用錯誤的標準答案閱卷,縱使及格,是否有效?近日更有專家從學術網站登出的高端報告看到,兩劑28天后的中和抗體效價在第二期受試者是662,爲第一期受試者52.2的12倍以上,差距如此大,恐無法單純以實驗室不同來解釋;而第一期的52.2,低於通過免疫橋接的門檻125.89(AZ效價187.9的0.67倍)。
在美國三款新冠疫苗中,拜登選擇接種混血的BNT疫苗,而非純美系的莫德納。梅克爾則在第一劑接種AZ後,第二劑混打莫德納,沒有打德國參與的BNT。日、韓在發展本土疫苗之外,代工AZ疫苗、大量採購國際疫苗,當疫情吃緊,不是趁火打劫、藉機闖關本土疫苗,而是積極催貨國際疫苗及使用代工的AZ過渡。他們都選擇科學與人權,超越「疫苗國族主義」。反觀臺灣,爲了意識形態,不肯採購BNT疫苗,而當民間積極爭取捐贈,還一卡再卡。總統捨棄國際疫苗不打,堅持施打本土疫苗也就罷了,但,代課教師、見實習生、入伍新兵何辜?年輕人何辜?總統的疫苗,未必是所有人的天菜。
若政府學習日、韓讓本土疫苗走完正當的科學流程,不僅免去超前核準帶來的質疑,更可在研發成功後銷售全世界,以更低單價供貨,達到更高總營收。除非是擔心禁不起考驗,否則名利雙收,何樂不爲?
當全球防疫邁向解封與正常化,臺灣卻執意豪賭,硬將私人廠商與愛臺灣畫上等號,進行情感勒索,甚至大剌剌進行政治動員,一旦發生問題,倒楣的是誰?對於未來的全民安全與經濟,更是投下未知的變數。
(作者爲國立陽明交通大學兼任教授)















